肠道微生态与自闭症谱系障碍科普
at 2026.03.18 22:48 ca 自闭症科普 pv 129 by 自闭症科普网
肠道微生态与自闭症谱系障碍:脑-肠-菌轴的双向调控机制、病理生理基础与临床干预路径深度研究报告
自闭症谱系障碍(Autism Spectrum Disorder, ASD)是一类高度异质性的神经发育障碍,临床核心特征主要表现为社交沟通障碍、受限的兴趣范围以及重复刻板的行为模式 [1, 2, 3]。在过去数十年间,ASD的全球患病率呈现显著上升趋势,最新的流行病学数据显示,部分地区的患病率已高达每36名儿童中就有1人被诊断为ASD,这一现象引起了公共卫生领域的高度关注 [4, 5]。尽管遗传因素在ASD的病因学中占据重要地位,已有超过100个基因被认为与自闭症风险相关,但单纯的遗传模型难以解释其复杂的表型多样性以及环境因素对病程的显著影响 [3, 5, 6]。
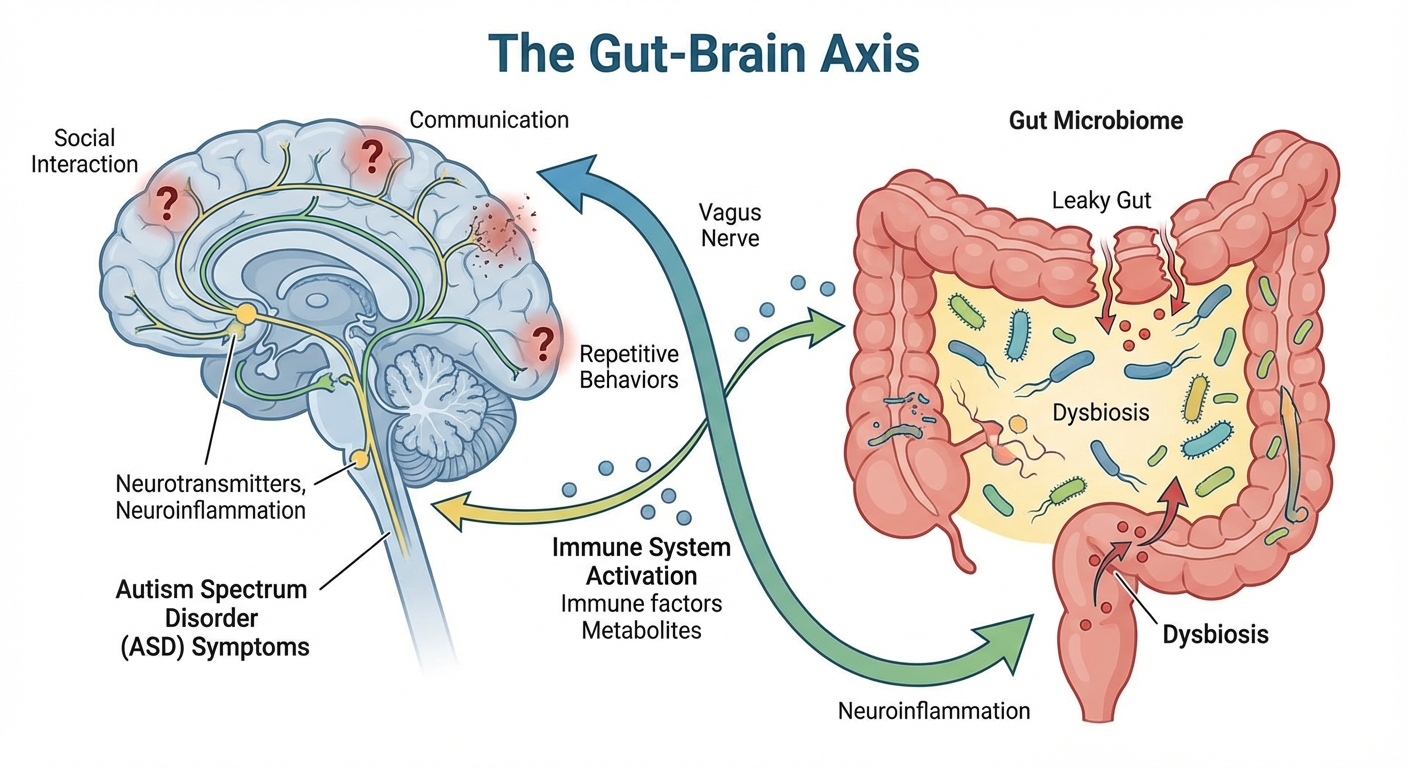
近年来,脑-肠-菌轴(Microbiota-Gut-Brain Axis, MGBA)的发现为理解ASD的病理生理机制开辟了全新的视角。研究表明,自闭症不仅仅是一种单纯的脑部疾病,更是一种涉及神经、免疫、内分泌及消化系统的全身性生理失调 [2, 7]。相当比例的ASD患者伴随慢性的胃肠道功能紊乱(Gastrointestinal Disorders),这些症状的严重程度往往与自闭症核心行为的严重性呈正相关,这促使科研界深入探索肠道微生物如何通过复杂的生物分子信号远程影响大脑功能 [1, 8, 9]。
脑-肠-菌轴的解剖学与生物学基础
肠道不仅是人体执行消化吸收功能的核心器官,其内部复杂的神经丛被称为“第二大脑”,即肠神经系统(Enteric Nervous System, ENS)。肠道中包含的神经元数量甚至超过了脊髓,这种解剖学上的复杂性为肠道与中枢神经系统(CNS)之间的高效通讯提供了基础 [10, 11]。脑-肠-菌轴是一个由神经、内分泌、免疫和代谢途径构成的双向通讯网络,通过这些通路,肠道微生物能够深刻调节宿主的脑发育、行为及认知功能 [2, 7]。
迷走神经的传入与传出动力学
迷走神经作为副交感神经系统的主要组成部分,是连接肠道与大脑最直接、最快速的通路。它由约80%的传入纤维和20%的传出纤维组成,其中传入纤维负责将肠道的物理和化学感应信号传输至大脑,而传出纤维则负责大脑对肠道功能的负反馈调节 [12]。肠道微生物通过产生神经活性代谢产物(如短链脂肪酸、神经递质等)直接或间接激活迷走神经传入末梢 [11, 12]。
值得注意的是,在肠脑之间的神经信号交换中,绝大部分(约90%)的信息是从肠道向大脑传导的,这种信息的不对称性表明肠道环境在很大程度上预设了大脑的某种功能状态 [10]。迷走神经还参与了著名的“胆碱能抗炎通路”,大脑通过迷走神经传出信号抑制外周炎症,并维持肠道通透性的稳态。如果这一通路受损,肠道微生物的组成将发生病理性偏移,进而通过反馈回路影响中枢神经系统的稳定性 [12]。
神经内分泌与递质调节通路
肠道微生物是调节宿主神经递质水平的重要“化工厂”。人体内超过95%的血清素(5-HT)产生于肠道,这种物质在调节情绪、社交能力、学习以及胃肠动力方面至关重要 [10]。自闭症患儿往往表现出色氨酸代谢通路的异常,色氨酸是合成血清素的前体,肠道微生物群落的失衡会导致色氨酸向血清素转化的路径受阻,进而影响大脑中神经递质的分布与浓度,这被认为是造成自闭症社交障碍和重复行为的生物学基础之一 [10, 13]。
此外,肠道微生物还能调节下丘脑-垂体-肾上腺(HPA)轴的活性。HPA轴是宿主应对压力的核心机制,肠道生态失调会导致皮质醇水平的异常波动,增强个体对应激环境的敏感性 [13]。对于自闭症个体而言,这种神经内分泌的紊乱往往外化为严重的焦虑情绪和对环境变化的过度反应 [8, 13]。
自闭症个体的肠道微生物特征
多项跨国、多中心的大规模宏基因组研究表明,ASD儿童的肠道微生物组成与发育典型(Neurotypical, NT)儿童存在显著且一致的差异。这种失衡不仅表现为特定致病菌的增加,还表现为益生菌丰度的显著下降以及整体物种多样性的缺失 [2, 14, 15]。
微生物丰度偏移与特定分类群
在门水平上,自闭症个体通常表现为厚壁菌门(Firmicutes)与拟杆菌门(Bacteroidetes)比例的失调,同时变形菌门(Proteobacteria)和疣微菌门(Verrucomicrobiota)的相对丰度往往有所上升 [15]。在更细微的属水平上,普拉梭菌(Faecalibacterium)和双歧杆菌(Bifidobacterium)等公认的有益菌显著减少,这些菌群在维持肠道抗炎环境和能量代谢平衡中起着支柱作用 [15]。
下表总结了目前研究中发现的自闭症个体肠道微生物的主要变化及其潜在影响:
| 微生物类别 | 变化趋势 | 相关的生理/病理影响 | 主要证据来源 |
|---|---|---|---|
| 双歧杆菌 (Bifidobacterium) | 显著减少 | 影响早期免疫系统成熟、叶酸合成以及对致病菌的防御 | [2, 6, 15] |
| 普拉梭菌 (Faecalibacterium) | 显著减少 | 导致丁酸产量下降,增加肠粘膜炎症风险 | [15] |
| 梭菌属 (Clostridium) | 显著增加 | 某些菌种(如破伤风梭菌)产生的毒素可经循环进入中枢,干扰行为 | [6, 16, 17] |
| 普氏菌属 (Prevotella) | 显著增加 | 与高丰度的某些炎症标志物相关,可能参与代谢异常 | [11, 15] |
| 阿克曼氏菌 (Akkermansia) | 相对增加 | 虽然在普通人中被视为有益,但在ASD群体中其异常比例可能影响粘液层稳态 | [15] |
| 脱硫弧菌 (Desulfovibrio) | 相对增加 | 产生硫化氢等代谢物,对肠细胞具有潜在毒性 | [2, 7] |
跨界别微生物组与病毒组的协同失调
最新的前沿研究(如香港中文大学团队的工作)已经将视野从单一的细菌域扩展到了古菌、真菌和病毒组。研究发现,自闭症个体的跨界别微生物网络不仅在组成上发生了变化,其内部的物种间通讯和代谢耦合也遭到了破坏 [14]。例如,肠道真菌群落的改变可能通过释放霉菌毒素进一步损害肠屏障,而噬菌体(病毒组的重要组成)的失衡则可能通过调节细菌群落的动态间接影响脑功能 [14]。
这种跨界别的微生物签名被证明具有极高的诊断潜力。通过机器学习算法筛选出的31种肠道微生物标志物,其诊断准确率在不同年龄、性别和地域的受试者中均保持了较高的灵敏度,为未来开发基于粪便样本的无创早期筛查工具提供了坚实的科学依据 [14]。
肠道通透性与神经免疫交互机制
在脑-肠-菌轴的调控模型中,肠道屏障的完整性被视为第一道防线。自闭症患者中普遍存在的“肠漏”(Leaky Gut)现象,使得肠道成为了全身炎症的源头 [2, 7, 18]。
连蛋白(Zonulin)与屏障功能的破坏
肠道上皮细胞间的紧密连接(Tight Junctions)是防止有害物质渗透的关键。连蛋白是目前已知的唯一一种生理性调节紧密连接通透性的蛋白质。在自闭症患儿的血浆中,连蛋白水平显著升高,且这一指标与患儿的社交受损程度及刻板行为的频率呈现出显著的正相关关系 [18]。连蛋白的上调预示着原本紧密的肠道屏障出现了“缝隙”,允许大分子物质、细菌产物及内毒素直接进入血液循环 [18]。
一旦肠道通透性增加,诸如脂多糖(LPS)、微生物相关分子模式(MAMPs)等强力促炎因子便会大规模渗透。这些物质通过循环系统到达血脑屏障(BBB),通过激活中枢神经系统的内皮细胞和星形胶质细胞,引起血脑屏障通透性的二次改变,最终导致神经炎症的发生 [18, 19, 20]。
慢性神经炎症与突触修剪
自闭症个体的神经免疫特征表现为持续的低度炎症状态。约60%的患者表现出明显的免疫功能紊乱,包括血液和脑脊液中促炎细胞因子(如IL-6、IL-17、TNF-α)的显著升高 [16, 20]。特别是IL-17,它在肠道中由特定的微生物(如分段丝状菌)诱导产生,能够直接影响大脑皮层的发育,干扰正常的突触修剪过程,这被认为是造成ASD个体大脑神经连接异常的核心机制之一 [16, 18]。
此外,自闭症患者体内常检测到针对大脑特定蛋白(如神经轴突丝蛋白、髓鞘碱性蛋白)的自身抗体。这些自身抗体可能通过分子模拟机制(Molecular Mimicry)产生,即由于肠道屏障破损,机体免疫系统在对某些细菌抗原产生免疫反应的同时,误伤了结构相似的脑组织蛋白,从而加剧了神经发育的偏离 [16]。
代谢组学揭示的化学通讯网络
肠道微生物产生的代谢产物是MGBA中最主要的生化介质。通过对自闭症患者尿液、血浆及粪便的代谢组学分析,研究者发现了一系列具有显著生物活性的特征代谢分子 [10, 16, 17]。
短链脂肪酸(SCFAs)的“双刃剑”作用
短链脂肪酸(主要是乙酸、丙酸和丁酸)是微生物发酵膳食纤维产生的初级代谢产物。在健康状态下,丁酸是肠道上皮的首选能量来源,并能通过上调紧密连接蛋白的表达来加固肠屏障,同时在脑内具有神经保护作用 [11, 20]。
然而,在自闭症个体中,SCFAs的平衡遭到破坏:
丙酸(Propionate)过量:过高浓度的丙酸具有一定的神经毒性,在啮齿类动物实验中,脑室内注射丙酸可直接诱发自闭症样的行为表型,如社交退缩和刻板动作,其机制涉及对线粒体功能的干扰和氧化应激的加剧 [11, 17]。
丁酸(Butyrate)缺乏:由于产丁酸菌(如普拉梭菌)的减少,肠道抗炎能力下降,这直接削弱了对神经系统发育的保护性支持 [11, 15]。
芳香族化合物与神经毒性
自闭症患者肠道中某些梭菌属细菌能通过代谢酪氨酸产生对甲酚(p-cresol)。这种小分子化合物具有较强的脂溶性,能穿过血脑屏障并抑制多巴胺-β-羟化酶的活性,从而改变大脑中多巴胺与去甲肾上腺素的平衡 [17]。这种神经化学环境的改变被认为与患者的社交动机受损和注意缺陷密切相关 [17, 21]。
此外,4-乙基苯酚硫酸盐(4-EPS)是另一种备受关注的微生物代谢物。实验显示,给予健康小鼠4-EPS足以诱导其产生明显的焦虑行为。通过调节肠道菌群(如补充脆弱拟杆菌)降低4-EPS水平,可以显著改善这些行为异常 [17, 22]。
胃肠道共病及其行为学意义
胃肠道症状是自闭症最常见的非核心特征,其在ASD人群中的患病率远高于普通人群。临床观察显示,90%以上的自闭症患者在生命周期的某个阶段会受到胃肠功能紊乱的困扰 [8, 23]。
GI症状的流行病学特征
自闭症患儿出现胃肠道问题的几率是神经典型发育儿童的4倍以上 [8]。常见的症状包括慢性便秘、反复腹泻、腹胀、腹痛以及胃食管反流 [9, 24]。这些症状不仅是消化系统的问题,更是整体生理失衡的外化表现。
下表根据多项元分析和系统评价,整理了自闭症人群中主要胃肠道症状的现患率:
| 胃肠道症状类型 | 估计现患率 | 对应的行为或情绪风险因素 | 文献支持 |
|---|---|---|---|
| 至少一种GI症状 | 48% - 70% | 与认知受损程度及自闭症评分负相关 | [4, 24] |
| 慢性便秘 | 34% - 37% | 增加攻击性行为、自伤风险及严重的焦虑感 | [8, 24, 25] |
| 反复腹泻 | 14% - 19% | 关联社交回避、易激惹和多动倾向 | [24, 25] |
| 腹痛/不适感 | 21% - 26% | 诱发突发性的情绪暴发和睡眠剥夺 | [8, 24, 25] |
| 胃食管反流 (GERD) | 显著高于对照组 | 与进食障碍及睡眠质量差高度相关 | [8, 26] |
疼痛的不可言说性与挑战性行为
对于许多存在语言发育迟缓或无言语沟通能力的自闭症患儿来说,胃肠道的物理疼痛无法通过常规语言表达,往往转化为“挑战性行为”(Challenging Behaviors),如自残、尖叫、无故的攻击性或异常的躯体姿势(如顶着腹部缓解疼痛) [8, 9, 27]。
临床证据一致表明,GI症状的严重程度与自闭症核心症状的评分(如CARS或ADOS评分)呈正向关联。这意味着,当患儿的肠胃问题得到有效管理时,其社交沟通意愿和学习适应能力往往会出现随之而来的提升 [9, 25, 28]。因此,胃肠道筛查应成为自闭症临床评估的常规组成部分,而非仅仅将其视为次要的共病 [25, 27]。
饮食偏好、因果倒置与“饮食中介模型”
尽管肠道微生态与自闭症的关联证据确凿,但一个核心的科学争议在于:究竟是菌群失调导致了自闭症,还是自闭症的特殊行为模式导致了菌群的改变?2021年发表在顶级期刊《细胞》(Cell)上的一项研究为此提供了重要的反向证据。
限制性饮食与微生物多样性的下降
自闭症个体的核心特征之一是“受限的兴趣和重复行为”,这在饮食领域表现为极度的食物选择性(Food Selectivity),受影响比例高达46%-89% [29]。由于对食物的纹理、颜色或气味的感官敏感,许多患儿仅愿意摄入极其有限的几类食物(如所谓的“米色饮食”:鸡块、白面包、薯条),这种偏好被证明与自闭症的多基因风险评分及社交损害程度密切相关 [30, 31]。
2021年的Cell研究通过对247名儿童的深度分析发现:
自闭症个体的肠道微生物多样性下降,主要是因为他们摄入的食物种类过少 [30]。
相比于自闭症诊断本身,饮食多样性和膳食纤维的摄入量更能解释微生物组成的变异 [30]。
这项研究提出了一个“逆向因果”模型:自闭症相关的行为特征(如刻板兴趣)导致了限制性饮食,进而引发了肠道菌群的改变。
这一发现对“肠道菌群驱动自闭症”的简单因果论提出了有力挑战,提醒我们在解读相关研究时必须充分考虑饮食这一混杂因素。然而,即便菌群改变是“果”,这种失调的菌群状态(如产生高浓度的神经毒性代谢物)仍可能反过来作为一个反馈环节,进一步恶化患者的行为表现,形成恶性循环 [7, 32]。
基于微生物组的治疗干预现状与前景
针对肠道生态系统的干预已成为自闭症辅助治疗的热点。目前的研究主要集中在益生菌、特定饮食限制以及更具突破性的粪菌移植技术。
益生菌(Probiotics)的应用
益生菌旨在通过引入活的有益微生物来调节肠道微环境。研究较多的菌株包括乳杆菌(Lactobacillus)和双歧杆菌(Bifidobacterium) [33, 34]。
临床效果:多项RCT研究显示,多菌株组合的益生菌产品在改善自闭症患儿的腹胀、便秘等GI症状方面效果明确。在行为方面,一些研究报告了患儿在焦虑、多动及自伤行为上的适度减轻,但对社交障碍等核心症状的长期改善仍缺乏足够强力的证据支持 [34, 35, 36]。
机制探索:动物模型显示,某些菌株(如L. reuteri)能通过激活迷走神经并诱导大脑中催产素(Oxytocin)的释放,从而显著改善个体的社交动机。然而,这一效应在人类群体中的重复性仍待验证 [22, 33]。
粪菌移植(FMT)与微生物转移疗法(MTT)
粪菌移植通过将健康供体的完整菌群植入患者肠道,试图实现微生态系统的全面重启。这是目前显示出最强效、最持久临床潜力的手段之一 [37, 38]。
长期获益:亚利桑那州立大学的一项标志性研究显示,经过两年的随访,接受微生物转移疗法(MTT)的自闭症患儿,其胃肠道症状缓解了约80%,且自闭症核心行为症状的严重程度下降了近50% [17, 37]。
洗涤微生物群移植(WMT):为了提升安全性,研究者开发了WMT技术,通过自动化清洗流程去除供体粪便中的促炎因子和非必要成分。初步证据显示,WMT能显著降低不良反应率,并有效改善患儿的感官敏感性和焦虑情绪 [39, 40]。
监管现状:尽管前景光明,但FMT/WMT目前在全球大部分地区仍属于临床研究阶段,尚未获得针对自闭症的正式临床指南推荐。FDA已发出多次安全警告,强调了供体筛选中对耐药菌和潜在病毒监测的极端重要性 [37, 41]。
特定饮食干预方案对比
家庭中应用最广泛的往往是各类排除饮食,其理论基础是减少肠道对潜在致敏原或神经毒素的吸收。
| 饮食干预类型 | 核心机制 | 对行为的潜在影响 | 临床风险与建议 | 文献 |
|---|---|---|---|---|
| 无麸质无酪蛋白 (GFCF) | 减少阿片样肽对大脑的干扰,降低促炎因子 | 改善注意力、多动及睡眠质量 | 易导致钙、维生素D及蛋白质缺乏,需定期监测 | [38, 42] |
| 生酮饮食 (KD) | 通过酮体提供替代能源,减少线粒体压力 | 显著减少癫痫发作频率,改善社交行为 | 存在肾结石、高脂血症等副作用,必须医学监督 | [5, 29, 43] |
| 低FODMAP饮食 | 减少可发酵糖类引起的肠内发酵和气压 | 缓解剧烈腹痛和腹胀,间接改善易激惹 | 属于极限制性饮食,容易导致营养不均衡 | [29, 44] |
| 特定碳水化合物饮食 (SCD) | 限制复合糖类,减少肠内病原菌增殖 | 减轻GI痛苦,提升整体生活质量 | 准备工作极其繁琐,家庭负担重 | [29] |
生物标记物与个体化营养
未来的干预将逐渐从“普遍化”转向“精准化”。例如,针对表现出色氨酸代谢障碍的患儿,补充特定的维生素B6、B9和B12可能更有效,因为这些辅因子是神经递质合成路径中必不可少的“催化剂” [29, 42]。同时,通过监测尿液中的对甲酚或4-EPS水平,可以帮助临床医生判断哪些患儿更可能从针对梭菌属的微生物疗法中获益 [17, 21, 34]。
政策、指南与公众认知的进化
随着脑-肠轴研究的普及,国际权威机构对自闭症的诊疗建议也在发生微妙的变化。美国儿科学会(AAP)和英国国家医疗服务体系(NHS)在维持审慎态度的同时,也开始强调对肠道健康的重视 [31, 45]。
权威机构的共识与声明
美国儿科学会 (AAP):其最新的政策声明强调,儿科医生应积极筛查自闭症患儿的胃肠道共病,并承认GI痛苦可能表现为各种挑战性行为。然而,对于GFCF等排除饮食,AAP仍建议仅在有明确食物不耐受证据的情况下应用,并须由注册营养师监控,以防止营养不良 [45, 46]。
英国国家儿科与健康研究所 (NICE):NICE指南目前不推荐将微生物制剂(益生菌)或复杂的饮食干预作为治疗自闭症核心症状的一线手段,理由是高质量的大规模随机双盲试验(RCT)数据仍显不足 [31]。
CDC与疫苗声明:针对长期存在的“疫苗导致自闭症并损害肠道”的谣传,美国CDC及全球主流传染病学会(如IDSA)多次重申,数十年间涉及数百万儿童的科学研究已彻底否定了疫苗(如MMR疫苗)与自闭症之间存在任何关联。任何反向宣传都被视为对公共卫生的严重威胁 [47, 48, 49]。
临床实践的综合管理模型
现代医学趋向于建立一个“全方位管理”模型。在该模型中,针对自闭症患儿的管理不再仅仅依赖传统的应用行为分析(ABA)等行为干预,而是将消化系统健康、睡眠调控、过敏管理和营养支持整合在一起 [27, 40]。通过改善患儿的物理舒适度(减少腹痛和炎症),可以为心理干预和教育训练提供更平稳的情绪底色,从而实现“身体舒适,行为改善”的协同效应 [9, 27, 32]。
结论与深度洞察
综上所述,肠道生态系统与自闭症谱系障碍之间存在着极其深厚且多层次的生物学关联。脑-肠-菌轴不仅是一个通讯系统,更是一个病理生理的交汇点。肠道微生物组的失衡,通过损害肠道和血脑屏障、释放代谢毒素以及引发全身神经免疫炎症,深刻地塑造了自闭症患者的行为景观。
核心结论摘要
双向互动的复杂性:肠道微生物既可能是自闭症神经发育异常的参与者(通过代谢物干扰脑功能),也可能是其特殊的饮食和行为模式的结果(饮食介导效应)。
GI症状的警示作用:胃肠道紊乱不仅是共病,更是自闭症严重程度的“放大器”。临床上必须重视将不明原因的情绪爆发与消化系统疼痛联系起来考虑。
代谢物作为关键介质:SCFAs、对甲酚和4-EPS等代谢产物是肠道向大脑传递有害信号的主要物质基础,是未来药物研发的潜在靶点。
干预手段的梯度性:膳食调整和益生菌补充被视为低风险的辅助手段,而粪菌移植(FMT)等强力干预虽然潜力巨大,但由于安全性和标准化问题,目前仍受限于临床研究范畴。
展望与未来挑战
未来的脑-肠-菌轴研究面临着几个关键性的挑战。首先是异质性问题:不同个体的自闭症遗传背景和菌群基准完全不同,这意味着“一刀切”的益生菌或饮食方案注定难以在所有人身上奏效。未来的趋势必将是基于多组学(基因组、宏基因组、代谢组)数据的个性化医疗。
其次,需要更深入地探索关键的“发育窗口期”。母体肠道微生物在妊娠期的状态对胎儿大脑发育的影响,以及婴儿出生后头三年的微生态建立过程,可能是预防或早期干预自闭症风险的“黄金期”。通过调控母婴菌群,或许能从根源上降低神经发育异常的发生率 [6, 29, 50]。
最后,脑-肠-菌轴的研究正在以前所未有的速度 subverting(颠覆)传统医学对大脑作为“免疫特权器官”的认知。肠道作为与外界环境接触面积最大的器官,其稳态的维持不仅是消化问题,更是中枢神经系统健康的核心基石。对于自闭症患者及其家庭而言,肠道健康的管理不仅是为了缓解便秘或腹泻,更是为了通过修复这一宏大的生物网络,为患儿争取更优质的神经发育轨道和生活质量。
免责与版权声明
每个“星星的孩子”都是独一无二的,本站分享的科普知识与干预经验仅供学习与交流,不能替代专业医疗机构的评估与诊断。
本站为公益博客,欢迎并鼓励非商业性转载与分享。转载时请注明文章出处,让我们一起传递科学与爱。