血脑屏障与自闭症谱系障碍因果
at 2026.03.19 00:09 ca 自闭症科普 pv 131 by 自闭症科普网
血脑屏障与自闭症谱系障碍:神经血管、免疫与肠-脑轴交织下的病理机制研究报告
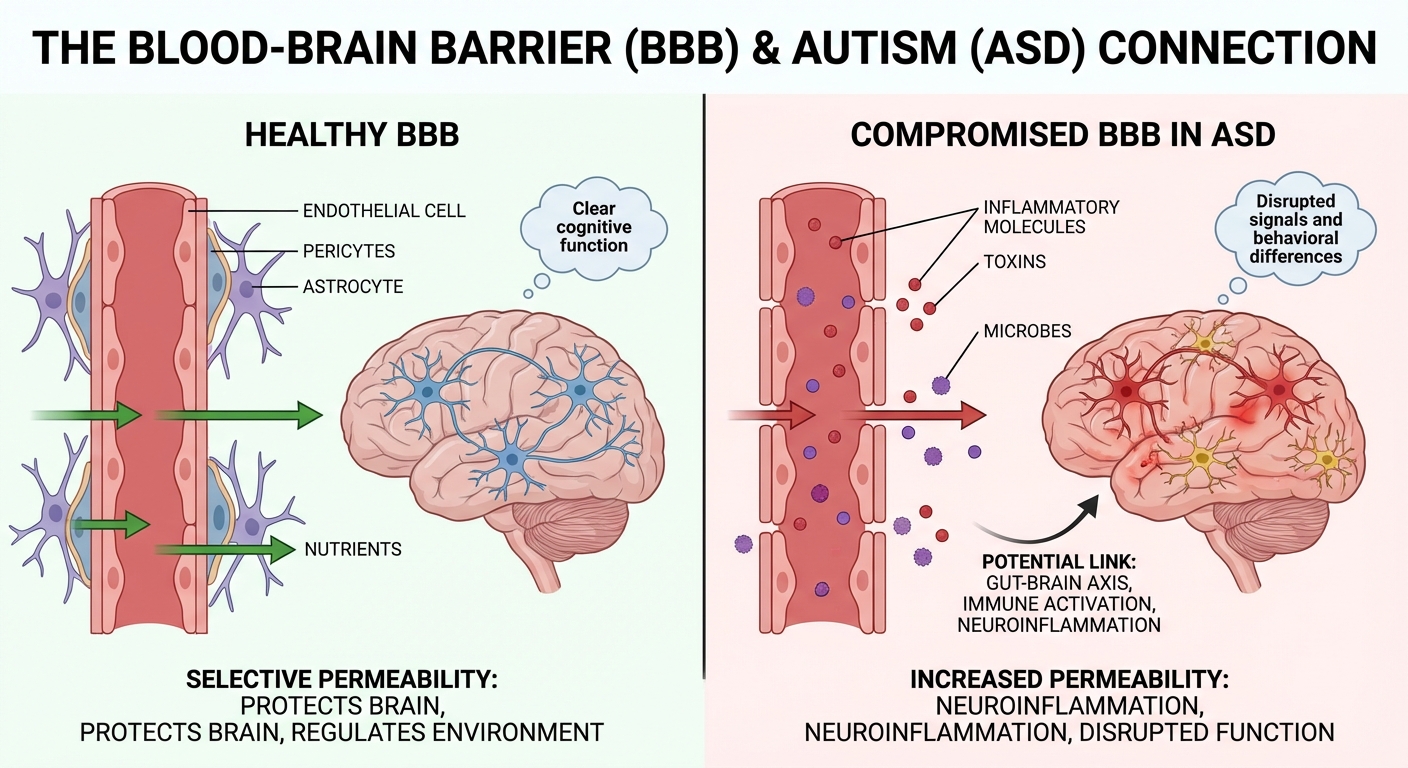
自闭症谱系障碍(Autism Spectrum Disorder, ASD)作为一类具有高度遗传和临床异质性的神经发育障碍,其病理机制的研究长期聚焦于突触连接异常、神经元迁移障碍以及兴奋/抑制性神经递质失衡。然而,随着神经血管生物学与免疫学的交叉研究不断深入,血脑屏障(Blood-Brain Barrier, BBB)在ASD发病过程中的核心角色日益凸显。血脑屏障不仅是中枢神经系统(CNS)与外周循环之间的简单物理屏障,更是维持大脑微环境稳态、调控免疫细胞浸润以及选择性转运关键代谢产物的动态功能复合体 [1, 2, 3]。本报告旨在系统性探讨血脑屏障在ASD中的发育障碍、结构破损、转运功能异常以及其与肠-脑轴和神经炎症的复杂交互作用,并评估其作为临床诊断与治疗靶点的潜力。
第一章 血脑屏障的生理基础与神经血管单元的整合功能
血脑屏障的结构完整性是由神经血管单元(Neurovascular Unit, NVU)内的多种细胞组分高度协调维持的。脑微血管内皮细胞(ECs)作为物理屏障的核心,其特征在于缺乏开孔且具有极低的胞吞作用率,而细胞间紧密连接(Tight Junctions, TJs)则赋予了其极高的跨内皮电阻 [1, 2, 4]。
1.1 紧密连接蛋白的分子构成及其动力学
紧密连接复合物是限制副细胞途径转运的关键。在ASD的研究背景下,特定的跨膜蛋白及其胞内支架蛋白表现出显著的表达差异。
| 紧密连接组成成分 | 关键分子 | 结构与生理功能 | ASD中的病理变异趋势 |
|---|---|---|---|
| 跨膜蛋白 (Claudins) | Claudin-5, -12, -3 | 形成选择性通透的密封链,直接决定屏障的物理致密性 [1, 5] | 皮层中Claudin-5与-12表达代偿性升高,提示原始屏障受损后的不稳态平衡 [6] |
| 紧密连接相关蛋白 | Occludin, Tricellulin | 增强连接的机械强度并参与信号转导,限制大分子跨屏障渗透 [1, 6] | Tricellulin在ASD皮层中表达上调,反映了神经血管单元对通透性改变的应激响应 [5] |
| 支架蛋白 | Zonula Occludens-1 (ZO-1) | 将跨膜蛋白锚定至肌动蛋白细胞骨架,维持极性与稳定性 [1, 7] | 在基因突变模型(如Cntnap2敲除)中表现为表达降低及排列紊乱 [7] |
| 功能调节酶 | MMP-9 (基质金属蛋白酶-9) | 降解基底膜与紧密连接蛋白,参与病理状态下的屏障破坏 [6, 8] | 在ASD脑组织中显著升高,预示着细胞外基质的持续降解与屏障不稳 [6, 9] |
1.2 神经血管单元的协同作用
除了内皮细胞,周细胞(Pericytes)与星形胶质细胞(Astrocytes)对于屏障的成熟与维护至关重要。周细胞包裹在血管表面,调节血管生成与基质沉积;星形胶质细胞足突则通过释放Sonic Hedgehog (Shh) 等神经营养因子,诱导内皮细胞表现出BBB特有的表型 [4, 10]。在ASD患者中,这种细胞间的对话机制往往在早期发育阶段就已受损,导致了“屏障生成(Barriergenesis)”的缺陷 [10]。
第二章 ASD发育过程中的血脑屏障生成信号通路障碍
ASD的病理生理过程往往起源于产前及早期产后的关键发育窗口期。在此阶段,血管生成与屏障生成的协调进行主要依赖于Shh与Wnt信号通路的复杂交互 [10]。
2.1 Sonic Hedgehog (Shh) 通路与屏障完整性
Shh信号在BBB的形成和维持中扮演着抗炎与屏障诱导的双重角色。星形胶质细胞分泌的Shh配体与其受体PTCH1结合,解除了对Smoothened (Smo) 的抑制,进而激活Gli转录因子 [10]。
屏障诱导机制: Shh通过诱导内皮细胞表达紧密连接蛋白(如Occludin和Claudin-5),增强了血管的封闭能力 [10]。
抗炎功能: 在健康状态下,Shh通路能有效抑制促炎因子和细胞间粘附分子-1(ICAM-1)的表达,从而阻止循环免疫细胞的非法浸润 [10]。
ASD中的异常: ASD患者中存在的Shh信号受损或PTCH1表达异常,直接导致了胶质激活与神经炎症的发生,使得BBB在发育早期即出现“渗漏”,允许外周毒性分子干扰神经元的定向迁移和突触连接的建立 [10]。
2.2 Wnt/β-catenin 信号的协同与拮抗
Wnt通路驱动了中枢神经系统特异性的血管形成。Wnt与Shh之间存在着精密的动态平衡:
协同互作: 两种通路的平衡控制着血管生成的速率与屏障生成的时机,确保在血管长入脑实质的同时,紧密连接结构同步形成 [10]。
交互调节: Wnt/β-catenin通路通过控制Gli3(Shh的主要阻断因子)下调Shh信号,而Shh则调节Wnt拮抗剂SFRP1来防止Wnt通路的过度激活 [10]。
突变影响: 临床研究发现,CHD8、CTNNB1、Wnt配体家族(如Wnt1, 2, 3等)的突变在ASD患者中高度富集。例如,CHD8的缺失会导致脑发育缺陷,这种缺陷可以通过稳定Wnt/β-catenin信号得到部分挽救 [10]。
第三章 遗传学证据:特定基因突变引发的屏障损伤
ASD的强遗传背景为其神经血管病理提供了坚实的证据基础。特定的高风险基因突变直接指向了BBB的结构受损或转运功能失效。
3.1 CNTNAP2 缺失与氧化应激驱动的屏障破坏
接触蛋白相关蛋白样2(CNTNAP2)被广泛认为是ASD的关键易感基因。在 Cntnap2 敲除(Cntnap2⁻/⁻)大鼠模型中,血脑屏障表现出明显的结构和功能崩溃 [7]。
通透性定性分析: 伊文思蓝(Evans Blue)和荧光素钠(FITC-dextran)检测显示,敲除鼠脑实质中出现了明显的染料渗漏,证实了屏障物理完整性的丧失 [7]。
分子病理特征: 免疫荧光显示ZO-1蛋白在脑血管上的排布不再连续,且整体水平显著下降 [7]。
氧化应激循环: Cntnap2⁻/⁻模型表现出严重的代谢紊乱,包括脂质过氧化指标TBARS的升高、抗氧化剂谷胱甘肽(GSH)的耗竭以及诱导型一氧化氮合酶(iNOS)的异常表达。这种氧化应激环境进一步加剧了血管内皮损伤,形成了“屏障破坏-炎症激活-氧化应激-屏障进一步受损”的恶性循环 [7]。
3.2 SLC7A5 (LAT1) 与氨基酸转运导致的代谢性ASD
血脑屏障的功能不仅在于屏蔽,更在于转运。SLC7A5(编码LAT1转运体)在BBB内皮细胞上高度表达,负责转运支链氨基酸(BCAA)等必需氨基酸 [4, 11]。
致病机制: 研究发现,SLC7A5 的纯合缺失会导致大脑内BCAA水平降至极低,即便外周血清水平正常。这直接损害了神经元的蛋白质合成和正常代谢 [11, 12, 13]。
表型关联: 携带该突变的ASD患者常伴有小头畸形(Microcephaly)和运动发育迟缓 [11, 14]。
干预启示: 这一发现具有里程碑意义,因为它证明了血脑屏障转运功能障碍可以是ASD的直接致病因素。在小鼠模型中,通过脑室内给药补充BCAA可以有效改善其自闭症样行为,这为精准医疗提供了新方向 [11, 12]。
3.3 22q11.2 缺失综合征中的内皮线粒体障碍
22q11.2缺失综合征患者中ASD的发病率极高。研究揭示,该区域缺失的基因中有多个编码线粒体蛋白。当这些蛋白在BBB内皮细胞中功能不全时,会导致内皮细胞能量代谢失败,进而引发血脑屏障渗漏 [15]。临床前证据显示,使用线粒体激动剂苯扎贝特(Bezafibrate)修复内皮线粒体功能,能够同步修复屏障完整性并缓解社会记忆缺陷 [15]。
第四章 肠-脑-屏障轴:全身性屏障失调的共病模型
自闭症研究中最为引人注目的理论之一是“漏肠-漏脑(Leaky Gut-Leaky Brain)”假说。ASD患者频繁出现的胃肠道症状(发病率高达70%)并非偶然,而是屏障系统整体性崩溃的体现 [16, 17, 18]。
4.1 肠道菌群失调与屏障同步受损
ASD患者的肠道微生态通常表现为生物多样性降低,具体表现为拟杆菌门(Bacteroidetes)减少和厚壁菌门(Firmicutes)与拟杆菌门的比例升高 [16, 18, 19]。
| 肠道/大脑区域 | 生化与分子改变 | 病理生理影响 |
|---|---|---|
| 肠道屏障 (Gut Barrier) | Claudin-1, Occludin 降低;Claudin-2, -10, -15 升高 [5, 6] | 肠道渗透性增加,导致LPS、食物抗原及细菌代谢产物进入体循环 [6, 16] |
| 循环系统 (Systemic) | 内毒素(LPS)、促炎细胞因子(IL−6,IL−17A)水平升高 [16, 18, 20] | 引发全身性低度炎症,激活BBB上的受体,下调内皮连接蛋白 [16, 20] |
| 血脑屏障 (BBB) | Claudin-5, -12 异常分布;MMP-9 降解作用增强 [6, 9] | 屏障封闭性丧失,允许外周炎症信号直接干扰脑部发育 [6, 21] |
4.2 微生物代谢产物的远端效应
微生物产生的代谢产物能够穿透受损的肠道屏障,并对BBB产生深远影响。例如,短链脂肪酸(SCFAs)在其中的作用具有双面性。
保护作用: 丁酸(Butyrate)和乙酸(Acetate)通常被认为能够加强血脑屏障的紧密连接。然而,在ASD患者中,产生丁酸的菌群(如 Prevotella)往往显著减少 [16, 21]。
毒性作用: 丙酸(Propionate)在ASD队列中常表现为水平升高。过量的丙酸能够干扰内皮细胞的氧化还原平衡,激活小胶质细胞并诱导神经炎症 [17, 21]。
色氨酸-犬尿氨酸通路: 菌群失调通过激活IDO1酶,将色氨酸代谢推向犬尿氨酸通路。这不仅降低了神经递质5-羟色胺(Serotonin)的合成,还产生了一系列具有神经毒性和BBB破坏作用的中间产物 [22, 23]。
第五章 母体免疫激活(MIA)与屏障发育的早期编程
环境压力源在产前阶段的影响往往通过母体免疫激活(MIA)这一机制实现。母体在怀孕期间的感染、自身免疫病或严重精神应激,会触发特征性的炎症反应,从而重塑胎儿的血脑屏障发育轨迹 [20, 24]。
5.1 IL-17A / IL-6 轴的核心作用
MIA诱导的母体细胞因子风暴是胎儿脑损伤的直接驱动力。
IL-17A 的致畸作用: 研究表明,来自母体Th17细胞的 IL-17A 可以穿过胎盘屏障。当其作用于胎儿大脑时,会激活神经祖细胞上的受体,导致皮层出现局部斑块状发育不良 [25]。同时,IL-17A 会抑制神经祖细胞向星形胶质细胞和少突胶质细胞前体(OPCs)的分化,从而损害未来的BBB结构支持系统 [20]。
IL-6 的干扰作用: 高水平的 IL-6 会导致神经祖细胞在短期内过度增殖,但在后期导致成人神经干细胞池的耗竭。这种失衡干扰了突触修剪和神经血管单元的精细构建 [20]。
5.2 屏障通透性的两种截然表型
不同的MIA模型在BBB通透性上呈现出不同的实验结果,这反映了环境影响的复杂性:
通透性增加表型: 在LPS或Poly I:C诱导的典型MIA模型中,子代BBB表现为高度通透,允许大量促炎因子进入脑部,引发持续的小胶质细胞激活 [20, 26]。
通透性降低(屏障硬化)表型: 在B族链球菌(GBS)诱导的绒毛膜羊膜炎模型中,研究者观察到胎儿BBB对白蛋白的渗透性反而显著降低,这伴随着紧密连接蛋白Claudin-5的异常升高 [27]。这种现象可能反映了一种早期应激下的“过度防御”,但由于破坏了大脑正常的营养与废物交换,同样会导致神经发育轨迹的偏离 [27]。
第六章 神经炎症与氧化应激:屏障损伤的持续催化剂
在ASD患者的脑组织中,神经炎症不仅是屏障受损的后果,更是其进一步恶化的催化剂。这一过程涉及胶质细胞的慢性激活和蛋白水解酶的过度分泌 [10, 28]。
6.1 反应性胶质增生与屏障动态平衡
小胶质细胞(Iba1): 活化的小胶质细胞会释放大量的 IL−1β,IL−6 和活性氧(ROS)。ROS能够直接攻击内皮细胞的脂质膜,而 IL−1β 则通过激活特定的激酶通路下调ZO-1的表达 [10, 28, 29]。
星形胶质细胞(GFAP): 虽然星形胶质细胞是BBB的支持细胞,但在炎症环境下,它们会发生反应性增生。此时,它们不仅丧失了分泌Shh的能力,还可能释放如S100B等促炎分子,进一步破坏内皮细胞的紧密连接 [10, 30, 31]。
6.2 基质金属蛋白酶(MMP)的破坏路径
MMP-9在ASD脑组织中的表达水平显著升高。这种酶具有降解基底膜(主要由IV型胶原蛋白组成)的能力。
物理剥离: MMP-9的过度激活会导致内皮细胞与基底膜脱离,破坏血管的结构支撑 [8]。
连接降解: MMP-9直接靶向并水解Claudin-5和Occludin,导致副细胞途径的门户大开,引发血管源性水肿和有害物质的大规模渗透 [6, 8]。
第七章 新兴环境压力源:微塑料与重金属的屏障穿透
随着环境污染的加剧,微塑料(Microplastics, MPs)作为一类新型环境风险因素,其对BBB的影响开始引起学界关注 [32]。
直接物理穿透: 动物实验显示,MPs能够穿透BBB并在脑组织中沉积。由于其不溶性和疏水性,MPs在脑血管内的蓄积会导致局部炎症和氧化应激 [32]。
毒理学机制: MPs暴露能够抑制乙酰胆碱酯酶(AChE)的活性,干扰胆碱能神经递质系统。同时,它们作为有毒重金属或环境内分泌干扰物的载体,协助这些物质跨越受损的屏障,加剧神经毒性 [32]。
二次打击: MPs通过引起肠道屏障损伤和菌群失调,触发全身性炎症。这种间接途径进一步削弱了BBB的防御能力,为ASD症状的加重提供了环境基础 [32]。
第八章 先进影像学与外周生物标志物:从临床科研到临床应用
由于难以直接获取活体ASD患者的脑组织,无创的影像学手段和外周生物指标成为了评估BBB状态的关键。
8.1 动态对比增强核磁共振(DCE-MRI)的应用
DCE-MRI是目前量化血脑屏障通透性的“金标准”。通过静脉注射钆对比剂(GBCA),监测其在脑组织中的渗漏速率 [2, 33]。
动力学模型: 利用Patlak图(Patlak Plot)计算流入常数(Ki)或容积转移常数()。公式可表达为:
PS=−ln(1−E)⋅f
其中 PS 是渗透性表面积乘积,E 是提取率,f 是脑血流量 [34]。临床发现: 虽然在ASD中的研究样本量较小,但初步证据显示,ASD患者在海马、丘脑等关键脑区存在微妙但具有统计学意义的对比剂渗漏。这不仅支持了BBB功能障碍的假说,也为分型诊断提供了工具 [2, 35]。
局限性与突破: 钆对比剂的安全性在儿科患者中一直备受关注。新兴的非对比剂技术,如基于动脉自旋标记(ASL)的水交换成像(WEPCAST MRI),正在被开发用于无创评估BBB对水分子的通透性 [34]。
8.2 外周血流体生物标志物
外周血中的某些蛋白水平可以间接反映中枢神经系统的屏障受损情况。
| 生物标志物 | 在ASD中的临床证据 | 诊断与病理意义 |
|---|---|---|
| S100B | 系统性综述显示,ASD患者外周血S100B水平显著高于对照组(p < 0.001) [30, 31] | 作为胶质细胞激活和BBB损伤的标志物,反映了脑实质成分向外周的溢出 [30] |
| GFAP | 血清GFAP水平与ASD核心症状的严重程度正相关 [31] | 提示神经血管单元中星形胶质细胞的病理性重构 [31] |
| NSE (神经元特异性烯醇化酶) | 尽管研究结果不一,但在多项研究中显示升高 [31] | 反映神经元受损及血脑屏障对其泄漏的允许性 [31] |
| QAlb (脑脊液/血清白蛋白比值) | 在精神疾病研究中被视为BBB通透性的经典指标 [35] | 虽然主要应用于成人研究,但其升高直接证据化了屏障的物理崩溃 [35] |
第九章 屏障修复:针对ASD的新型治疗策略探讨
鉴于血脑屏障在ASD病理中的中心地位,修复和保护屏障完整性成为了极具潜力的干预方向。
9.1 分子靶向与药物干预
Rho激酶(ROCK)抑制剂: 法舒地尔(Fasudil)在多种模型中显示出能通过抑制神经炎症和调节内皮细胞极性来修复BBB [36]。
线粒体保护: 针对22q11.2缺失模型,使用苯扎贝特等PPAR激动剂提升内皮细胞线粒体能量水平,显示出稳定紧密连接的显著效果 [15]。
Sonic Hedgehog 激动剂: 增强Shh通路信号有助于在炎症环境下维持屏障的抗炎属性,目前正作为神经保护药物进行探索 [10]。
9.2 肠-脑轴同步修复
靶向益生菌: 补充具有增强屏障功能的菌株(如 Bifidobacterium infantis)可以降低血清中LPS水平,从而减轻其对BBB的攻击 [16, 22]。
饮食方案: 严格的无麸质、无酪蛋白(GFCF)饮食在部分患儿中有效,其原理可能是通过降低肠道源性促炎因子的负荷,间接改善了大脑的稳态环境 [9, 37]。
粪菌移植(FMT): 虽然仍处于临床试验阶段,但初步数据显示其对ASD行为症状的改善与肠道屏障功能的恢复密切相关 [17]。
9.3 免疫调节与预防
母体炎症干预: 在孕期监测并控制炎症水平(如通过合理运动、抗炎饮食或必要的药物干预),阻断 IL-6/IL-17A 信号通路,可能是预防神经发育风险的关键 [20, 25]。
大麻二酚 (CBD) 的应用: CBD展现出的多靶点抗炎作用,不仅能调节胶质细胞活性,还可能通过调节血管内皮舒缩功能保护屏障 [38]。
第十章 总结与展望
血脑屏障在自闭症谱系障碍中的角色已经从单纯的病理后果演变为复杂病理网络中的关键节点。本报告通过综合遗传学、免疫学、肠道微生物组学以及先进影像学的证据,构建了一个多维度的病理模型:
第一,血脑屏障的缺陷在ASD中表现为“发育编程”与“持续损伤”的并存。从胚胎期的Shh/Wnt信号失调,到生后持续的神经炎症攻击,屏障系统的脆弱性贯穿了ASD的全生命周期。
第二,“屏障共病”是ASD患者系统性表现的基础。肠道屏障与血脑屏障的协同受损,使得大脑不再是一个“免疫特权区”,而是暴露在来自环境和肠道的各种复杂信号冲击之下。
第三,代谢转运体的特异性故障(如SLC7A5案例)揭示了BBB作为“代谢守门人”的功能缺失可以直接诱发孤独症表型。这不仅深化了我们对ASD致病机理的认识,也为“屏障代谢疗法”奠定了理论基础。
未来的研究应致力于:1) 开发更高分辨率、非侵入性的BBB功能影像技术,以捕捉临床早期微妙的通透性变化;2) 探索个体化医疗,识别哪些患者的症状主要由屏障受损驱动;3) 验证多靶点干预策略,将神经修复与屏障修复有机结合。血脑屏障不再仅仅是一道墙,而是一扇窗,通过这扇窗,我们或许能找到理解和治愈自闭症的新路径。
报告中使用的来源
Blood-brain barrier and intestinal epithelial barrier alterations in autism spectrum disorders
Altered Blood Brain Barrier Permeability and Oxidative Stress in ...
Blood-brain barrier and intestinal epithelial barrier alterations in autism spectrum disorders
Blood-brain barrier and intestinal epithelial barrier alterations in autism spectrum disorders
the amino acid transporter LAT1 (SLC7A5) in the Blood-Brain Barrier - CNR-IRIS
Potential Crosstalk between Sonic Hedgehog-Wingless-related ...
the amino acid transporter LAT1 (SLC7A5) in the Blood-Brain Barrier - CNR-IRIS
Blood-brain barrier and intestinal epithelial barrier alterations in autism spectrum disorders
Blood-brain barrier and intestinal epithelial barrier alterations in autism spectrum disorders
Maternal Immune Activation and Neurodevelopmental Disorders ...
Maternal Immune Activation and Neurodevelopmental Disorders ...
Maternal Immune Activation and Neurodevelopmental Disorders ...
Potential Crosstalk between Sonic Hedgehog-Wingless-related ...
Potential Crosstalk between Sonic Hedgehog-Wingless-related ...
Potential Crosstalk between Sonic Hedgehog-Wingless-related ...
Imaging blood-brain barrier permeability through MRI in pediatric sickle cell disease - PMC
Blood–brain barrier and intestinal epithelial barrier alterations in ...
Maternal Immune Activation and Neurodevelopmental Disorders ...
Cannabidiol and Neurodevelopmental Disorders in Children - PMC - NIH
免责与版权声明
每个“星星的孩子”都是独一无二的,本站分享的科普知识与干预经验仅供学习与交流,不能替代专业医疗机构的评估与诊断。
本站为公益博客,欢迎并鼓励非商业性转载与分享。转载时请注明文章出处,让我们一起传递科学与爱。